出生缺陷严重影响国民健康。有数据显示,当前已知的出生缺陷病种超过8000种,其中神经管畸形是常见的一类出生缺陷。出生缺陷的发生与早期胚胎发育异常直接相关。因此,研究早期胚胎发育过程、探究发育机理,是揭示病理性胚胎发生机制,提升相关疾病诊疗效率,从根源上提高人民健康水平的重要前提。
人早期胚胎发育起始于受精卵(胚胎期第0天;day post-fertilization 0;d.p.f. 0)。受精卵经过数次卵裂形成囊胚,囊胚于d.p.f. 7左右种植入母体子宫并进一步发育,于d.p.f. 14启动原肠运动。原肠运动是早期胚胎发育过程中的里程碑事件,在此过程中,胚胎细胞发生大规模分化、迁移和重排,并形成外、中、内三胚层和体轴。外胚层于d.p.f. 20左右进一步发育形成位于中间的神经板(也称为神经外胚层)、位于两侧的表皮外胚层和位于两者之间的神经板边缘。神经板弯曲、折叠、增厚并进一步闭合,形成神经管。闭合的神经管沿胚胎背腹轴分化出不同的神经祖细胞。神经管形成的过程称为神经胚形成。中、内胚层进一步发育出体节、心脏、肠管等早期器官的原基,胚胎自此进入更加复杂的器官发育阶段。由于人早期胚胎样品极难获取,以上事件在人类胚胎中无法被直接探究和揭示。
胚胎体外培养技术为探究人类胚胎早期发育提供了有力武器。借此,人d.p.f. 14之前的发育事件已被初步揭示1-4。但人类胚胎体外研究存在必须在d.p.f. 14终止的伦理限制。因此,体外培养的人类胚胎不能被用于研究d.p.f. 14之后的原肠运动和早期神经胚发育等事件。非人灵长类与人类在进化上和发育生物学特征上高度相似,是研究人早期胚胎发育的理想模型。因此,搭建非人灵长类胚胎体外培养体系,揭示非人灵长类胚胎发育特征,将极大提升我们对包括人类在内的灵长类早期胚胎发育及相关疾病的认识。1995年,澳大利亚科学家将绒猴的囊胚体外培养至d.p.f. 11,用于研究灵长类动物胚胎植入后发育5。2019年,王红梅团队及国内外同行将食蟹猴胚胎体外培养至d.p.f. 20,探究了灵长类早期原肠运动特征6,7。那么,灵长类胚胎中晚期原肠运动和早期神经胚发育有哪些特征?是否可以延长食蟹猴胚胎体外发育历程,以进一步探究灵长类胚胎发育特征?这些问题一直是发育生物学领域前沿热点问题。
为了回答以上科学问题,研究者建立了一个可支持食蟹猴胚胎体外发育至受精后25天的3D长时程培养体系,并基于该体系探究了灵长类胚胎中晚期原肠运动和早期神经发育过程中的核心事件和谱系特征。研究者比较了人类和非人灵长类胚胎2D(2D Ibidi μ-plates和2D coated with Matrigel, Ibidi-2D和M-2D)和3D(3D low-adhesion 96-well with Matrigel, M-3D)体外培养体系1,6,7,对不同体系中胚胎的大小和存活率进行评估。研究者发现,2D和3D体系都能支持胚胎发育到d.p.f. 20。在2D体系下,胚胎由于胚外组织发育旺盛而迅速增大,但内部的胚体发育并不好。而在3D体系下,胚胎的胚外组织生长受限,但胚体结构显著发育。这些特征提示2D体系优先支持胚外组织生长,而胚外组织的过度生长可能限制了胚体本身的发育。为了保证胚体的发育,研究者继续优化3D体系。已报道的人类胚胎M-3D体系需要在d.p.f. 9-14的培养基中连续添加Matrigel,以模拟人类胚胎植入后环境1。鉴于食蟹猴胚胎植入子宫比人类胚胎浅表,因此,研究者仅在d.p.f. 10-12的培养基中加入Matrigel。优化后的体系能支持33.7%(n = 91)的食蟹猴胚胎发育到d.p.f. 25,该体系被命名为3D长时程培养体系(prolonged in vitro culture,pIVC;图1)。
为了探究灵长类早期神经胚发育过程,研究者首先对神经系统发育关键调控因子进行鉴定。首先,d.p.f. 20-22胚胎的胚体背侧中部可检测到OTX2+/OCT4+或OTX2+/SOX2+的细胞,提示OTX2的表达与外胚层细胞分化密切相关。PAX3和PAX6表达于d.p.f. 22-25的外胚层细胞,表明此时神经外胚层的特化。在d.p.f. 24-25的胚胎中可检测到神经外胚层闭合的区域,提示神经管形成。另外,OTX2、PAX8和NKX2.2阳性细胞分布于神经管的前部、中部和后部,提示此时的胚胎已有前脑、中脑和后脑/脊髓的区域化。结合神经管的形态特征,研究者发现胚胎前部神经管未闭合,后部神经管已闭合。未闭合和已闭合的神经管都表达N-CAD,而不表达E-CAD,表明胚胎在神经管闭合之前已完成E-CAD向N-CAD的转变。这些pIVC胚胎的神经管形态和分子表达特征与体内相同发育阶段的胚胎相似(图2)。伴随神经外胚层的发育,表皮和神经板边缘的发育同步进行。荧光染色结果显示,d.p.f. 22-25的胚胎已分化出TFAP2A+/E-CAD+的表皮细胞。在未闭合的神经板两侧和闭合的神经管两侧存在PAX3+/SOX9+/SLUG+细胞,标志着神经板边缘和其分化的神经嵴细胞的发育。
为了探究闭合的神经管细胞是否具有沿背腹轴不对称分化的模式,研究者对d.p.f. 25胚胎的神经管进行鉴定。发现在闭合的神经管背侧存在PAX3阳性细胞、腹侧存在FOXA2和NKX6.1阳性细胞,表明神经管顶板(roof plate)和底板(floor plate)的特化。此外,β-tubulin Ⅲ+/OLIG2+细胞标志着运动神经元祖细胞(progenitors of motor neurons)的特化;NKX2.2+/FOXA2+细胞标志着腹侧中间神经元祖细胞(progenitors of ventral interneuron 3)的特化。与闭合的神经管相比,OLIG2和NKX2.2未能在未闭合的神经管中检测到。这些分子表达特征与体内对应阶段胚胎的特征一致,表明pIVC胚胎可重现神经管沿背腹轴区域化发育的模式(图3)。
除外胚层和神经管发育外,研究者还检测了pIVC胚胎中原始生殖细胞(primordial germ cells)和中、内胚层的发育特征。荧光染色结果显示,SOX17+/TFAP2C+/BLIMP1+细胞可在d.p.f. 22-24的胚胎后部腹侧被检测到,提示pIVC胚胎可发育出原始生殖细胞样细胞。在胚胎腹侧的位置还可检测到T+/CDX2+/OCT4+/Low或T+/TBX6+/SOX2-细胞,表明pIVC胚胎可发育出原条及其分化产物。此外,T+/TBX6+/SOX2+细胞的出现提示胚体存在类神经中胚层祖细胞(neuromesodermal progenitor)或前体节中胚层细胞(presomitic mesoderm)的特化。另外,研究者可在pIVC胚胎的单细胞转录组数据中检测到MYL7、NKX2-5、HAND1和GATA4共表达的细胞,提示pIVC胚胎或存在心脏中胚层样细胞。单细胞多组学和荧光染色结果提示pIVC胚胎中可检测到OTX2+/FOXA2+/SOX17+细胞,表明胚胎已分化出定型内胚层(definitive endoderm)和卵黄囊(yolk sac)。与相同发育阶段的体内正常胚胎相比,pIVC胚胎的这些分子表达特征与正常胚胎相似,表明pIVC胚胎可重现原肠运动中晚期阶段中胚层和内胚层的发育。
研究者进一步利用单细胞多组学测序技术(单细胞转录组、DNA甲基化和染色质可及性测序,scChaRM-seq)8,对9个pIVC胚胎的3,850个单细胞的转录组和1,862个单细胞的DNA甲基化和染色质可及性进行测序和分析。结果提示,与本团队2022年在Nature杂志报道的相同发育阶段的食蟹猴胚胎单细胞转录组数据库相比9,pIVC胚胎可重现体内正常胚胎的转录组特征。DNA甲基化分析提示,pIVC胚胎各种细胞类型的基因均发生了甲基化,且胚胎组织的DNA甲基化水平(~75%)高于胚外组织(~50%),这与已报道的小鼠和人类胚胎特征相似2,10。
综上所述,本研究建立了可支持食蟹猴胚胎体外发育至d.p.f. 25的3D pIVC体系,基于该体系揭示了灵长类胚胎中晚期原肠运动至早期神经胚发育阶段胚胎的形态、细胞组分、转录组、DNA甲基化和染色质可及性等特征。该研究为深入了解人类早期胚胎发育机制,以及早期胚胎发育异常相关疾病的病理研究提供了技术平台。
本研究工作于2023年5月11日以封面文章形式发表于Cell,题为“Neurulation of the cynomolgus monkey embryo achieved from 3D blastocyst culture”。中国科学院动物研究所王红梅研究员、美国宾夕法尼亚大学Nicolas Plachta教授、中国科学院动物研究所郭帆研究员和李伟研究员为该文共同通讯作者。中国科学院动物研究所副研究员翟晶磊、博士研究生徐艳红、助理研究员万海峰、博士研究生燕蕊、博士研究生郭敬以及美国宾夕法尼亚大学博士后Robin Skory为该文的共同第一作者。
文章链接:https://www.cell.com/cell/fulltext/S0092-8674(23)00415-4
参考文献:
1 Xiang, L. et al. A developmental landscape of 3D-cultured human pre-gastrulation embryos. Nature 577, 537-542, doi:10.1038/s41586-019-1875-y (2020).
2 Zhou, F. et al. Reconstituting the transcriptome and DNA methylome landscapes of human implantation. Nature 572, 660-664, doi:10.1038/s41586-019-1500-0 (2019).
3 Shahbazi, M. N. et al. Self-organization of the human embryo in the absence of maternal tissues. Nat Cell Biol 18, 700-708, doi:10.1038/ncb3347 (2016).
4 Deglincerti, A. et al. Self-organization of the in vitro attached human embryo. Nature 533, 251-254, doi:10.1038/nature17948 (2016).
5 A. Lopata, D. J. K., L.G. Bowes, AND W.B. Watkins. Culture of Marmoset Blastocysts on Matrigel: A Model of Differentiation During the Implantation Period. THE ANATOMICAL RECORD 241, 469-486 (1995).
6 Ma, H. et al. In vitro culture of cynomolgus monkey embryos beyond early gastrulation. Science 366, doi:10.1126/science.aax7890 (2019).
7 Niu, Y. et al. Dissecting primate early post-implantation development using long-term in vitro embryo culture. Science 366, doi:10.1126/science.aaw5754 (2019).
8 Yan, R. et al. Decoding dynamic epigenetic landscapes in human oocytes using single-cell multi-omics sequencing. Cell Stem Cell 28, 1641-1656 e1647, doi:10.1016/j.stem.2021.04.012 (2021).
9 Zhai, J. et al. Primate gastrulation and early organogenesis at single-cell resolution. Nature 612, 732-738, doi:10.1038/s41586-022-05526-y (2022).
10 Argelaguet, R. et al. Multi-omics profiling of mouse gastrulation at single-cell resolution. Nature 576, 487-491, doi:10.1038/s41586-019-1
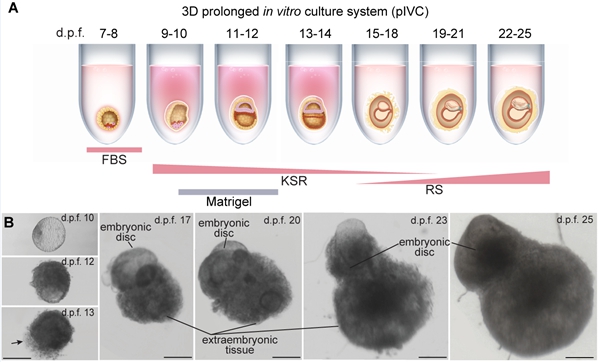
图1. 能够支持食蟹猴胚胎体外发育至d.p.f. 25的3D长时程培养体系
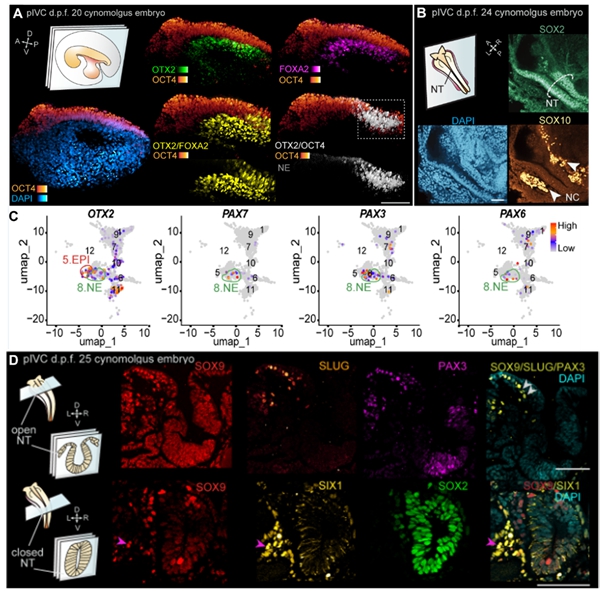
图 2. pIVC胚胎神经外胚层和神经嵴的特化
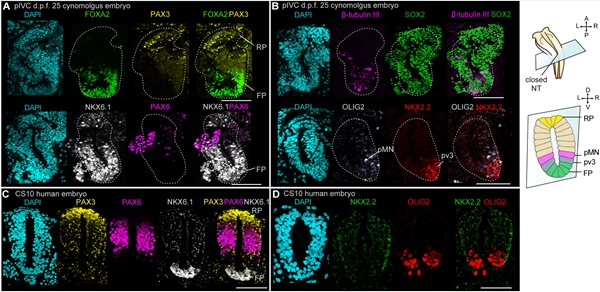
图3. pIVC胚胎神经管细胞的特化

