| 本组致力于女性生殖与疾病的研究。主要研究方向为细胞命运决定、胎盘发育与生理和病理的妊娠结局。 本组致力于女性生殖与疾病的研究。主要研究方向为早期胚胎发育、胎盘发育与生理和病理的妊娠结局、干细胞与女性生育力的维持和重建。 早期胚胎发育与成功妊娠密切相关,团队多年来致力于哺乳动物胚胎体外培养体系的优化,结合仿生材料、动态培养体系、实时监测系统等条件的搭建和完善,目前可将小鼠囊胚体外长时程培养至E8.5阶段,人类囊胚体外长时程培养至E14,非人灵长类囊胚体外培养至E20阶段。其中“利用食蟹猴胚胎体外长时程培养体系研究灵长类动物早期原肠运动特征的研究”于2019年发表于science杂志。 胎盘绒毛滋养层细胞的合体化及对子宫内膜的适当侵润是成功妊娠的关键,其异常将导致自然流产、葡萄胎、先兆子痫和胎儿生长受限(FGR)等病理事件。生殖生理组通过利用人胎盘绒毛滋养层细胞侵润/转移和合体化、胚胎-子宫内膜共培养、小鼠胎盘特异敲低或敲除等模型结合蛋白质组学和单核苷酸基因多态性等方法研究胎盘早期发育和滋养层细胞分化的分子机制及相关疾病的发病机理。 原始卵泡库从根本上决定了雌性生育力,原始卵泡激活和卵泡发生控制着生殖和生理周期。卵泡发育异常在临床上可引发卵巢早衰(POF)和多囊卵巢综合症(PCOS)等多种生殖疾病,严重威胁女性生育力。生殖生理组首先应用化疗药物制造小鼠卵巢功能不全模型(POI),随后进行干细胞注射治疗小鼠POI,验证干细胞治疗的安全性和有效性,通过转录组学,代谢组学等研究卵泡发育和生育力维持的的分子机制,并将这种疗法运用于临床前研究。 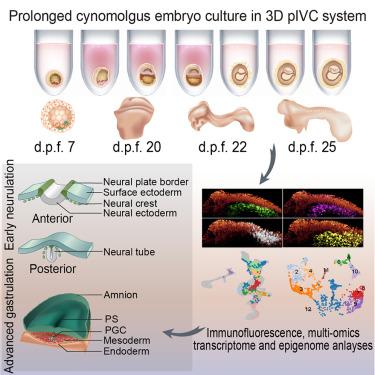
Zhai JL, et al. 通过3D囊胚培养实现食蟹猴胚胎的神经形成. Cell. 2023

Zhai JL, et al. 食蟹猴胚胎单细胞转录组学揭示原肠胚形成和早期器官发生. Nature. 2022

Gu Z, et al. 受子宫启发的生态位推动囊胚发育到早期器官发生. Advance Science. 2022
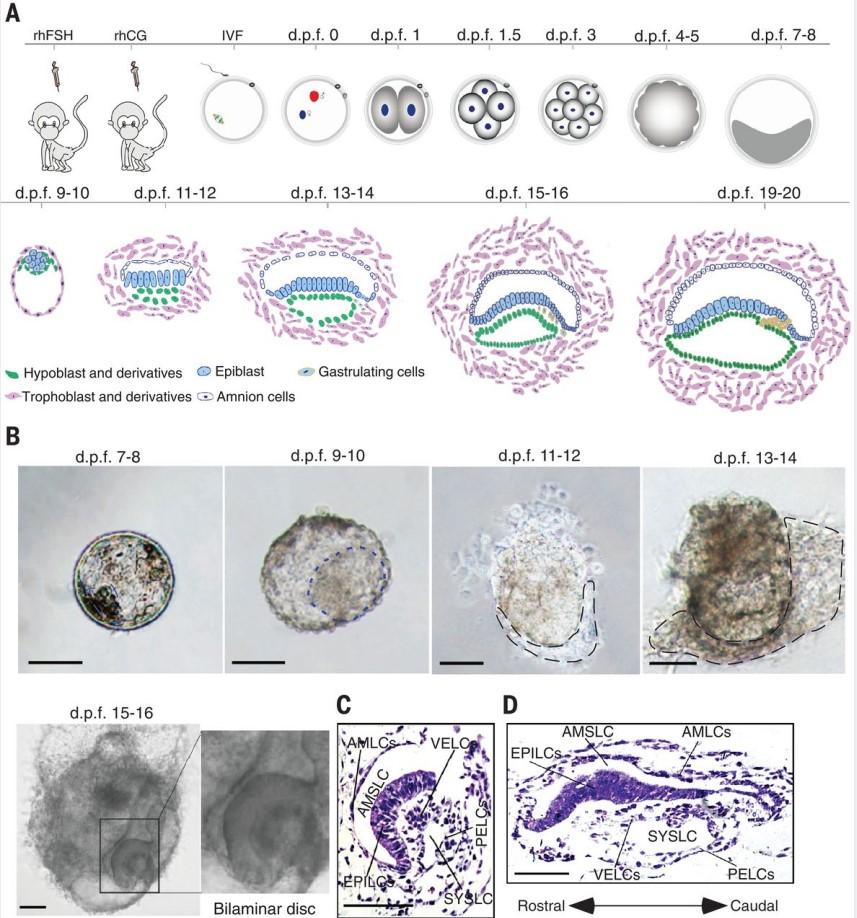
Ma H, et al. 食蟹猴早期原肠胚的体外培养. Science. 2019
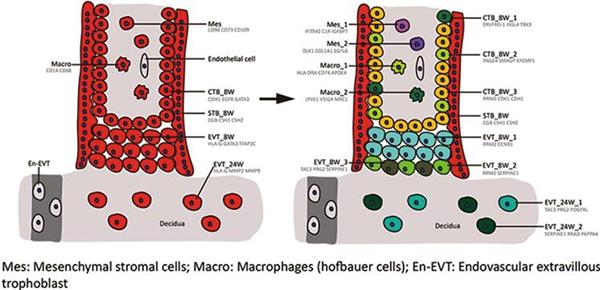
Liu Y, et al. 单细胞RNA-seq揭示了滋养细胞亚型在人胎盘的多样性和分化模式. Cell Research, 2018

Chang WL, et al. Plac8是人类间质外滋养细胞的新标记物,可促进细胞的侵袭和迁移. Development, 2018
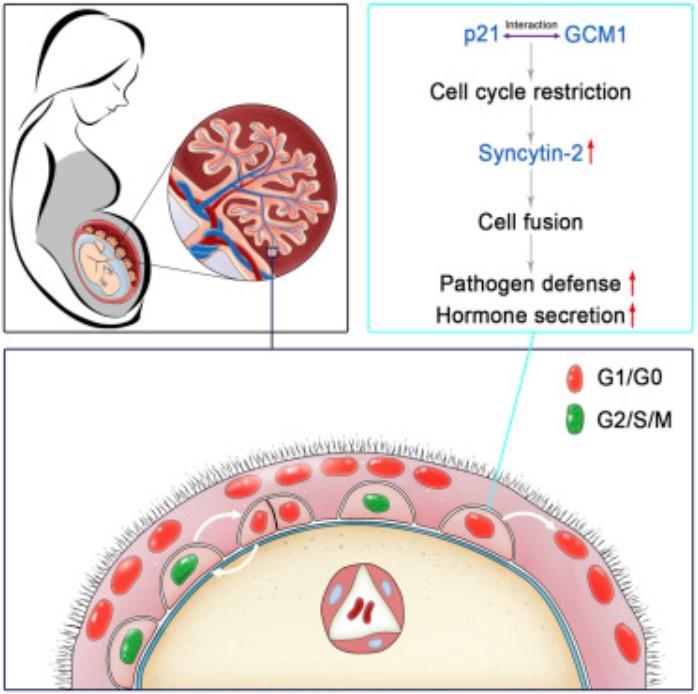
Lu X, et al. 精细调控和细胞周期限制的融合蛋白Syncytin-2的表达维持胎盘合胞体的功能. Cell Reports. 2017
| 研究内容和目标:
本课题组致力于女性生殖健康研究。集中研究妊娠过程中胚胎早期发育的分子机理以及胎盘发育和妊娠维持的分子机理,以及卵巢功能与妊娠结局的关系:(1)早期胚胎发育与成功妊娠密切相关,我们利用人、食蟹猴和小鼠等模型研究胚胎早期发育、胎盘发育及其相关疾病的发病机理;(2)正常的哺乳动物卵泡发生是周期性排出健康且可受精卵子的可靠保障。卵泡激活发育异常在临床上可引发卵巢早衰(POF)和多囊卵巢综合症(PCOS)等生殖疾病,严重威胁妇女健康。我们运用小鼠和灵长类动物模型以及临床人类疾病资源,揭示卵泡发育和生育力维持的分子机理。 代表性发表论文: - Yu D#, Wan H#, Tong C#, Guang L#, Chen G#, Su J#, Zhang L, Wang Y, Xiao Z, Zhai J, Ma W, Liang K, Liu T, Wang Y, Peng Z, Luo L, Yu R, Li W*, Qi H*, Wang H*, Shyh-Chang N*. A multi-tissue metabolome atlas reveals core signatures and critical nodes of metabolic reprogramming in female primates during pregnancy. Cell. 2024, 187, 764-781 e714.1.
- Wang M#, Liu Y#, Sun R#, Liu F#, Li J, Yan L, Zhang J, Xie X, Li D, Wang Y, Li S, Zhu X, Li R*, Lu F*, Xiao Z*, Wang H*. Single-nucleus multi-omic profiling of human placental syncytiotrophoblasts identifies cellular trajectories during pregnancy. Nat Genet. 2024, 56, 294-305.
- Wang Y#, Deng W#, Lee D#, Yan L#, Lu Y, Dong S, Huntoon K, Antony A, Li X, Ye R, Zhao Y, Zhao F, Schrank BR, Ha J, Kang M, Yang M, Gong P, Lorenzi PL, Tan L, Gallup TD, Tang SK, Yang Z, Li J, Sanford NN, Wang H*, Kim BYS*, Jiang W*. Age-associated disparity in phagocytic clearance affects the efficacy of cancer nanotherapeutics. Nat Nanotechnol. 2024,19, 255-263.
- Wu H#, Zhai J#, Wang H*. Unraveling the function of FGF signaling in human hypoblast specialization. Cell Stem Cell. 2024, 31(7):945-946. (comments)
- Yu X#, Wu H#, Su J#, Liu X, Liang K, Li Q, Yu R, Shao X, Wang H*, Wang YL*, Shyh-Chang N*. Acetyl-CoA metabolism maintains histone acetylation for syncytialization of human placental trophoblast stem cells. Cell Stem Cell. 2024, 31(9):1280-1297.e7.
- Wu X#, Zhai J#, Li Q#, Wang H*. The in vitro culture of mammalian embryos. Nat Method.2023, 20, 1855-1858. (comments)
- Wu H#, Huang XY#, Sun MX#, Wang Y#, Zhou HY#, Tian Y#, He BJ, Wu AP, Wang H*, Qin CF*. Zika virus targets human trophoblast stem cells and prevents syncytialization in placental trophoblast organoids. Nat Commun. 2023, 14, 5541.
- Zhai J#, Xu Y#, Wan H#, Yan R#, Guo J#, Skory R#, Yan L, Wu X, Sun F, Chen G, Zhao W, Yu K, Li W*, Guo F*, Plachta N*, Wang H*. Neurulation of the cynomolgus monkey embryo achieved from 3D blastocyst culture. Cell. 2023, 186(10). cover story.
- Jiang X #, Zhai J #, Xiao Z#, Wu X#, Zhang D#, Wan H, Xu Y, Qi L, Wang M, Yu D, Liu Y, Wu H, Sun R, Xia S, Yu K, Guo J, Wang H*. Identifying a dynamic transcriptomic landscape of the cynomolgus macaque placenta spanning during pregnancy at single-cell resolution. Dev Cell. 2023 Apr; 58:806-821.
- Jiang X#*, Wang Y# , Xiao Z, Yan L, Guo S, Wang Y, Wu H, Zhao X, Lu X*, Wang H*. A differentiation roadmap of murine placentation at single-cell resolution. Cell Discov. 2023 Mar;9(1):30.
- Zhai J#, Guo J#, Wan H#, Qi L#, Liu L#, Xiao Z, Yan L, Schmitz DA, Xu Y, Yu D, Wu X, Zhao W, Yu K, Jiang X*, Guo F*, Wu J*, Wang H*. Primate gastrulation and early organogenesis at single-cell resolution. Nature. 2022 Dec;612(7941):732-738.
- Zhou JJ#, Jiang XX#, Wu HW#, Zhang LJ, Chen M, Chen M, Shen ZM, Guo XD*, Wang H*, Gao F*, Dissecting the fate of 1 Foxl2-expressing cells in fetal ovary using lineage tracing and Single-Cell Transcriptomics. Cell Discov. 2022 Dec;8(1):139.
- Yan R#, Cheng X#, Gu C#, Xu YH#, Long X#, Zhai JL, Sun FY, Qian JJ, Du YR, Wang H*, Guo F*, Dynamics of DNA hydroxymethylation and methylation during mouse embryonic and germline development. Nat Genet. 2023 Jan, 55(1):130-143.
- Li Q#, Wu H#, Wang Y, # Wang H*, Current understanding in deciphering trophoblast cell differentiation during human placentation. Biol Reprod. 2022, 107(1):317-326. Review
- Gu Z#, Guo J#, Zhai J#, Feng G, Wang X, Gao Z, Li K, Ji S, Wang L, Xu Y, Chen X, Wang Y, Guo S, Yang M, Li L,Hua H, Jiang L, Wen Y, Wang L, Hao J, Li W, Wang S,* Wang H*, Gu Q*. A Uterus-Inspired Niche Drives Blastocyst Development to the Early Organogenesis. Adv Sci. 2022,10.1002.
- Tu W#, Ni D#, Yang H#, Zhao F#, Yang C#, Zhao X#, Guo Z#, Yu K, Wang J, Hu Z, Chen Z, Zhao Y, Wang Z, Gao F, Yan L*, Yang X*, Zhu L*, Wang H*. Deciphering the dynamics of the ovarian reserve in cynomolgus monkey through a quantitative morphometric study. Sci Bull. 2022, 67(18): 1854-1859.
- Wang Y#, Jiang X#, Jia L#, Wu X#, Wu H#, Wang Y, Li Q, Yu R, Wang H*, Xiao Z*, Liang X*. A Single-Cell Characterization of Human Post-implantation Embryos Cultured In Vitro Delineates Morphogenesis in Primary Syncytialization. Front Cell Dev Biol. 2022 Jun 15;10:835445.
- Wang Y#, Wu H#, Jiang X#, Jia L#, Wang M, Rong Y, Chen S, Wang Y, Xiao Z*, Liang X*, Wang H*. LMNA Determines Nuclear Morphology During Syncytialization of Human Trophoblast Stem Cells. Front Cell Dev Biol. 2022 Apr 11;10:836390.
- Zhai J#, Xiao Z#, Wang Y#, Wang H*. Human embryonic development: from peri-implantation to gastrulation. Trends Cell Biol. 2022 Jan;32(1):18-29. Review
- Liang G#, Zhou C#, Jiang X#, Zhang Y, Huang B, Gao S, Kang Z, Ma D, Wang F, Gottgens B*, Wang H*, Han JJ*, Liu F*. De novo generation of macrophage from placenta-derived hemogenic endothelium. Dev Cell. 2021 Jul 26;56(14):2121-2133.
- Wu H#, Liao S#*, Wang Y#, Guo M#, Lin X, Wu J, Wang R, Lv D, Wu D, He M, Hu B, Long R, Peng J, Yang H, Yin H, Wang X, Huang Z, Lan K, Zhou Y, Zhang W, Xiao Z, Zhao Y*, Deng D*, Wang H*. Molecular evidence suggesting the persistence of residual SARS-CoV-2 and immune responses in the placentas of pregnant patients recovered from COVID-19. Cell Prolif. 2021 Sep;54(9):e13091.
- Yan R#, Gu C#*, You D, Huang Z, Qian J, Yang Q, Cheng X, Zhang L##, Wang H##, Wang P*, Guo F*. Decoding dynamic epigenetic landscapes in human oocytes using single-cell multi-omics sequencing. Cell Stem Cell. 2021, 28(9):1641-1656.e7.(##Senior author)
- Li X#, Wang Y#, Ma R#, Liu X, Song B, Duan Y, Guo J, Feng G, Cui T, Wang L, Hao J*, Wang H*, Gu Q*. Reconstruction of functional uterine tissues through recellularizing the decellularized rat uterine scaffolds by MSCs in vivo and in vitro. Biomed Mater. 16 (2021) 035023.
- Qu Y#, Chen Q#, Guo S#, Ma C, Lu Y, Shi J, Liu S, Zhou T, Noda T, Qian J, Zhang L, Zhu X, Lei X, Cao Y, Li W, Li W, Plachta N, Matzuk MM, Ikawa M, Duan *E, Zhang Y*, Wang H*. Cooperation-based sperm clusters mediate sperm oviduct entry and fertilization. Protein Cell. 2021 Oct;12(10):810-817.
- Zhao Y#, Ma J#, Yi P#, Wu J#, Zhao F, Tu W, Liu W, Li T, Deng Y, Hao J*, Wang H*, Yan L*. Human umbilical cord mesenchymal stem cells restore the ovarian metabolome and rescue premature ovarian insufficiency in mice. Stem Cell Res Ther. 2020 Nov 4,11(1),466.
- Yan L#, Wu Y#, Li L#, Wu J#, Zhao F, Gao Z, Liu W, Li T, Fan Y*, Hao J*, Liu J*, Wang H*. Clinical analysis of human umbilical cord mesenchymal stem cell allotransplantation in patients with premature ovarian insufficiency. Cell Prolif. 2020, 53(12), e12938.
- Xiao Z#, Yan L#, Liang X*, Wang H*. Progress in deciphering trophoblast cell differentiation during human placentation. Curr Opin Cell Biol. 2020, 18(67), 86-91. (invited review)
- Lim HYG, Alvarez YD, Gasnier M, Wang Y, Tetlak P, Bissiere S, Wang H, Biro M, Plachta N*. Keratins are asymmetrically inherited fate determinants in the mammalian embryo. Nature. 2020, 585(7825), 404-409.
- Ma H#, Zhai J#, Wan H#, Jiang X, Wang X, Wang L, Xiang Y, He X, Zhao ZA, Zhao B, Zheng P*, Li L*, Wang H*. In vitro culture of cynomolgus monkey embryos beyond early gastrulation. Science.2019, 366(6467): eaax7890.
- Guo S#, Cui X#, Jiang X#, Duo S, Li S, Gao F*, Wang H*. Tracing the origin of the placental trophoblast cells in mouse embryo development. Biol Reprod. 2020 Mar 13;102(3):598-606.
- Wang R#, Yu R#, Zhu C, Lin HY, Lu X*, Wang H*. Tubulin detyrosination promotes human trophoblast syncytium formation. J Mol Cell Biol. 2019, 11(11), 967-978. (cover story)
- Ma J#, Wu J#, Han L, Jiang X, Yan L, Hao J*, Wang H*. Comparative analysis of mesenchymal stem cells derived from amniotic plate under serum-free condition. Stem Cell Res Ther. 2019, 10(1), 19.
- Liu Y#, Fan X#, Wang R#, Lu X#, Dang YL, Wang H, Lin HY, Zhu C, Ge H, Cross JC*, Wang H* Single-cell RNA-seq reveals the diversity of trophoblast subtypes and patterns of differentiation in the human placenta. Cell Res. 2018, 28(8), 819-832.
- Jiang X, Du MR, Li M, Wang H*. Three macrophage subsets are identified in the uterus during early human pregnancy. Cell Mol Immunol. 2018, 15(12), 1027-1037.
- Chang WL#, Liu YW#, Dang YL#, Jiang XX, Xu H, Huang X, Wang YL, Wang H, Zhu C, Xue LQ, Lin HY, Meng W*, Wang H*. Plac8, a new marker for human interstitial extravillous trophoblast cells, promotes their invasion and migration. Development. 2018, 145(2), dev148932.
- Lu X#, Wang R#, Zhu C, Wang H, Lin HY, Gu Y, Cross JC*, Wang H*. Fine-Tuned and Cell-Cycle-Restricted Expression of Fusogenic Protein Syncytin-2 Maintains Functional Placental Syncytia. Cell Reports. 2017, 21(5), 1150-1159.
|

